CIRURGIA FETAL
Síndrome da Transfusão Feto-Fetal (STFF): diagnóstico, tratamento e cirurgia fetal a laser
A síndrome da transfusão feto-fetal (STFF) é uma complicação grave das gestações gemelares monocoriônicas, causada por conexões vasculares anormais na placenta compartilhada. Sem tratamento, a mortalidade pode se aproximar de 100% nos casos graves. A cirurgia fetal a laser — que coagula essas conexões — é hoje o tratamento de referência e mudou radicalmente o prognóstico dessa doença.
Em resumo
- A STFF afeta 10-15% das gestações gemelares monocoriônicas e se manifesta geralmente entre 15 e 26 semanas
- O diagnóstico é feito por ultrassom, com base na discrepância de líquido amniótico entre os gêmeos e alterações no Doppler
- A cirurgia fetal a laser (fetoscopia) elimina a causa da doença ao coagular as anastomoses placentárias
- O laser oferece sobrevida de ao menos um gemelar em 76% dos casos, contra 51% da amniodrenagem (Senat 2004, NEJM)
O que é a Síndrome da Transfusão Feto-Fetal
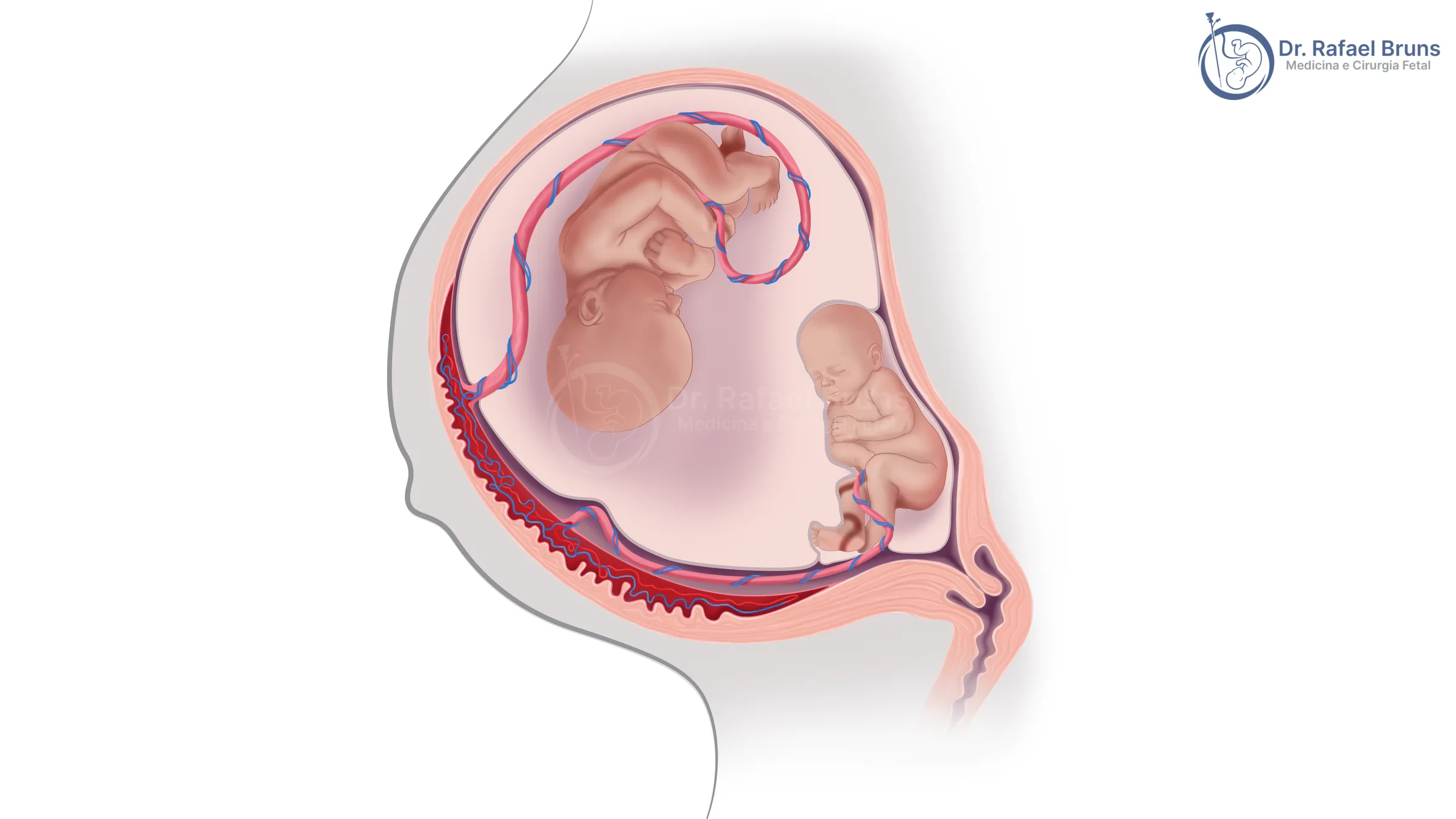
A síndrome da transfusão feto-fetal — também conhecida pela sigla em inglês TTTS (twin-to-twin transfusion syndrome) — é uma complicação exclusiva das gestações gemelares monocoriônicas, ou seja, aquelas em que os gêmeos compartilham uma única placenta. Ela afeta entre 10% e 15% dessas gestações e costuma se manifestar entre 15 e 26 semanas de gestação.
Na transfusão feto-fetal, conexões vasculares anormais na superfície da placenta — chamadas anastomoses — criam um desequilíbrio no fluxo sanguíneo entre os dois fetos. Um dos gêmeos (o doador) perde volume de sangue para o outro (o receptor), de forma contínua e progressiva. Sem tratamento, a STFF grave pode levar ao óbito de ambos os bebês. Nos casos graves diagnosticados antes da 28ª semana, a mortalidade fetal pode superar 80% sem intervenção. A STFF é, por isso, considerada uma condição de elevada morbimortalidade fetal e neonatal — e uma das principais indicações de cirurgia fetal no mundo.
Justamente por causa dessa gravidade, a STFF foi uma das primeiras condições fetais para as quais se desenvolveu tratamento cirúrgico intrauterino — a cirurgia fetal a laser ou ablação de anastomoses vasculares. A possibilidade de intervir durante a gestação, eliminando a causa do problema na placenta, transformou o prognóstico dessa doença.
Uma história pessoal com a STFF
Meu primeiro contato com a transfusão feto-fetal foi em 2001, durante a residência. Uma paciente de 17 anos chegou com STFF grave — e os dois bebês não sobreviveram. Naquela época, o laser simplesmente não existia no Brasil. A impotência diante de uma doença para a qual já existia tratamento em outros países foi determinante na minha trajetória.
Em 2015, completei o Advanced Course in Fetoscopic Laser Surgery no Leiden University Medical Center, na Holanda, com o Prof. Dick Oepkes — um dos maiores especialistas mundiais em cirurgia fetal a laser. Do caso sem opção terapêutica à formação no centro que desenvolveu a técnica — essa trajetória resume o que a medicina fetal avançou em pouco mais de uma década.

Linha do tempo — marcos na história da STFF
Esaú e Jacó — relato bíblico possivelmente compatível com STFF (Ville 1997, Berger 2000). Ler mais ↓
De Wikkelkinderen — pintura holandesa com possível representação visual da transfusão feto-fetal (Berger et al., Lancet 2000). Ler mais ↓
Friedrich Schatz descreve a "terceira circulação" em placentas gemelares. Ler mais ↓
Schatz publica a descrição completa da síndrome no Archiv für Gynäkologie.
Julian De Lia realiza a primeira coagulação a laser das anastomoses placentárias por fetoscopia (FLOC). Ler mais ↓
Rubén Quintero publica o sistema de estadiamento em 5 estágios (J Perinatol).
Dr. Rafael Bruns acompanha seu primeiro caso de STFF durante a residência — perda dos dois bebês, sem laser disponível no Brasil. Ler mais ↓
Senat et al. publicam no NEJM o ensaio randomizado que prova a superioridade do laser sobre a amniodrenagem. Ler mais ↓
Dr. Rafael Bruns e Dr. Fábio Peralta realizam a primeira cirurgia fetal fetoscópica para STFF do Sul do Brasil — procedimento inédito na região.
Técnica de Solomon validada em ensaio clínico (Slaghekke et al., Lancet) — Leiden como centro de referência. Ler mais ↓
Dr. Rafael Bruns completa o Advanced Course in Fetoscopic Laser Surgery em Leiden, com o Prof. Dick Oepkes — um dos maiores especialistas mundiais em cirurgia fetal a laser.
Primeira cirurgia fetal em Curitiba — marco importante na consolidação do serviço de cirurgia fetal no Paraná.
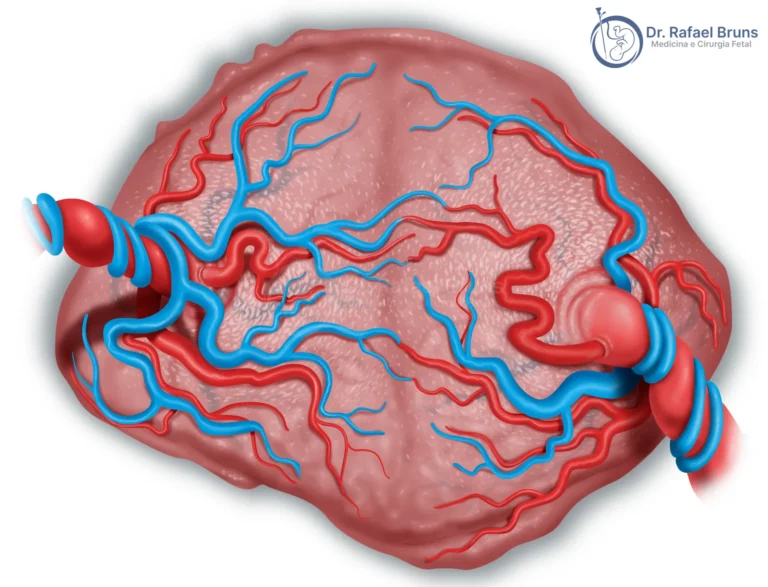
Como a STFF acontece na placenta
Para entender a transfusão feto-fetal, é preciso entender a placenta monocoriônica. Em gestações gemelares monocoriônicas, os dois bebês compartilham uma única placenta. Na superfície dessa placenta, existem vasos que conectam os territórios de cada feto — as chamadas anastomoses vasculares.
Em uma gestação monocoriônica sem complicações, essas conexões costumam ser equilibradas: o que um feto envia ao outro, o outro devolve por outra via. O fluxo nos vasos sanguíneos placentários e no cordão umbilical de cada feto permanece estável, sem diferença significativa de volume entre os dois. Quando esse equilíbrio se rompe — predominando anastomoses arteriovenosas em uma só direção — o fluxo sanguíneo passa a favorecer sistematicamente um dos gêmeos.
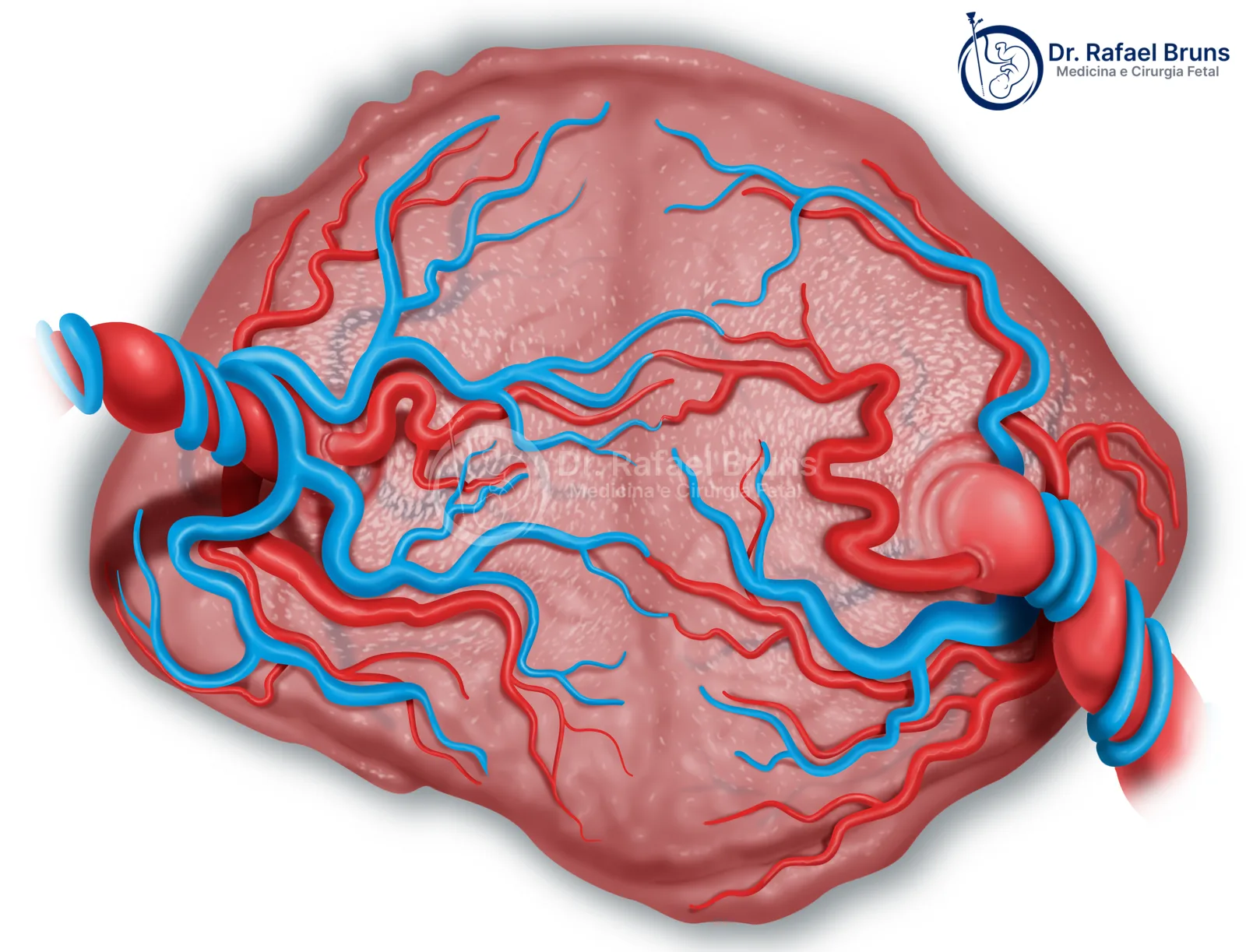
Feto doador e feto receptor: o que acontece com cada um
Feto doador: perde volume sanguíneo progressivamente. Seus rins produzem menos urina, o líquido amniótico ao seu redor diminui drasticamente (oligodrâmnio) e ele pode ficar aprisionado pela membrana — o chamado stuck twin (gêmeo preso). Quando temos um stuck twin, o gemelar aprisionado fica como se tivesse sido "embalado a vácuo" pela membrana. A membrana que separa os gêmeos torna-se de difícil identificação por estar comprimida contra o corpo do gêmeo doador. Há risco de desidratação, anemia e insuficiência renal.
Feto receptor: recebe excesso de sangue. Seus rins tentam compensar produzindo mais urina, acumulando líquido amniótico em excesso (polidrâmnio). A sobrecarga circulatória pode levar à insuficiência cardíaca, hidropsia fetal e, em última instância, ao óbito.
É essa dinâmica — um feto perdendo e o outro recebendo demais — que dá nome à síndrome. O problema não está nos fetos em si, mas nas conexões vasculares da placenta que compartilham. Apesar dos pais terem grande preocupação com o feto doador, na verdade em geral é o receptor que tem um quadro mais grave pois pode apresentar insuficiência cardíaca em função do aumento de volume sanguíneo.
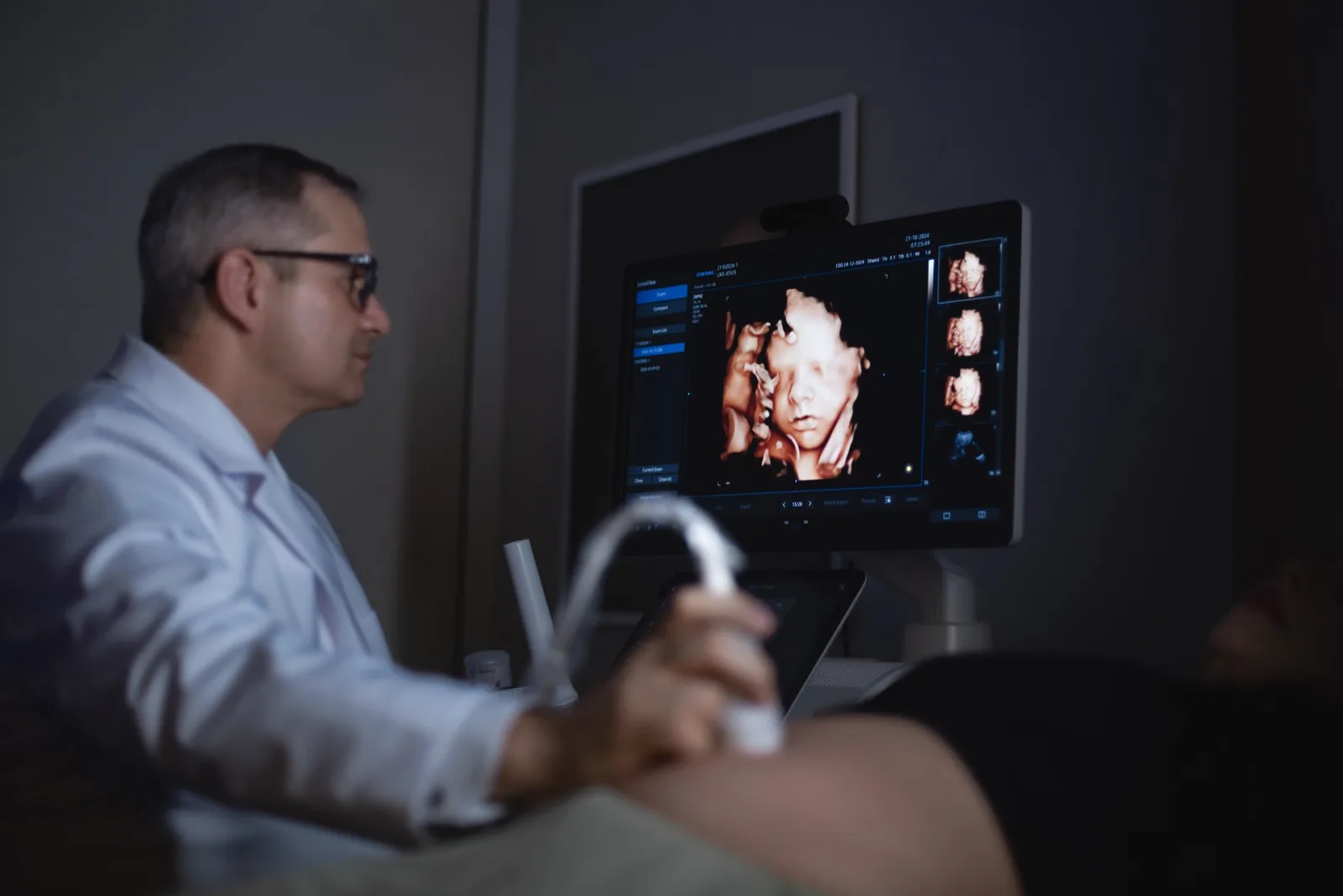
Quais são os sinais da STFF no ultrassom
Como identificar a síndrome de transfusão feto-fetal precocemente
O diagnóstico da síndrome da transfusão feto-fetal é feito por ultrassom. Os sinais são característicos e, em mãos experientes, permitem identificar a doença com segurança. Os principais achados incluem:
- Discrepância no líquido amniótico: o sinal mais marcante — polidrâmnio (excesso de líquido) no saco do receptor e oligodrâmnio (redução acentuada) no saco do doador
- Bexiga do doador não visualizada: como o doador produz pouca urina, a bexiga pode não ser identificada ao ultrassom
- Stuck twin (gêmeo preso): o doador fica imobilizado pela membrana contra a parede uterina, pela ausência de líquido ao seu redor
- Alterações no Doppler: fluxo ausente ou reverso na artéria umbilical do doador, pulsatilidade anormal no ducto venoso
- Sinais de sobrecarga cardiovascular no receptor: cardiomegalia, regurgitação de valvas cardíacas, hidropsia fetal nos casos avançados
É por isso que, em toda gestação gemelar monocoriônica, o acompanhamento ultrassonográfico deve ser feito a cada duas semanas a partir de 16 semanas — para detectar a STFF o mais precocemente possível, quando o tratamento tem melhores resultados.
Classificação de Quintero
Em 1999, o médico Rubén Quintero e colaboradores publicaram no Journal of Perinatology um sistema de estadiamento que até hoje é a referência para classificar a gravidade da STFF. São cinco estágios progressivos:
| Estágio | Achados |
|---|---|
| I | Discrepância de líquido amniótico (polidrâmnio/oligodrâmnio), porém a bexiga do doador ainda é visível |
| II | Bexiga do feto doador não visualizada ao ultrassom |
| III | Alterações no Doppler — fluxo ausente/reverso na artéria umbilical, pulsatilidade anormal no ducto venoso ou veia umbilical |
| IV | Hidropsia fetal — acúmulo anormal de líquido em cavidades do corpo do feto (geralmente no receptor) |
| V | Óbito de um ou ambos os fetos |
O estadiamento de Quintero orienta diretamente a decisão terapêutica. A partir do estágio II, a cirurgia fetal a laser costuma ser indicada. No estágio I, a conduta expectante — com acompanhamento ultrassonográfico rigoroso a cada 1–2 semanas — pode ser adotada quando não há sinais de deterioração clínica, pois uma parcela dos casos estabiliza espontaneamente. No estágio II, a bexiga do doador não é visualizada ao ultrassom, caracterizando o chamado stuck twin — o gêmeo doador fica imobilizado pela membrana, sem líquido ao seu redor. A partir do estágio III, as alterações dopplervelocimétricas nos vasos umbilicais ou no ducto venoso indicam comprometimento hemodinâmico significativo e reforçam a indicação cirúrgica. Nos casos de estágios III e IV com inviabilidade técnica do laser ou gestação muito precoce, o feticídio seletivo pode ser discutido como alternativa para preservar o gemelar saudável — uma decisão que envolve considerações éticas, clínicas e familiares complexas.
Quando a cirurgia fetal a laser é indicada
A cirurgia fetal a laser — tecnicamente chamada de fetoscopia com coagulação a laser das anastomoses placentárias — é o tratamento de referência para a STFF grave. A indicação principal é a transfusão feto-fetal a partir do estágio II de Quintero, diagnosticada antes de 26 semanas de gestação. A janela terapêutica ideal para o laser situa-se entre 18 e 26 semanas — antes desse período o acesso fetoscópico é tecnicamente mais difícil; após esse limite, o risco de parto prematuro imediato aumenta. Nos casos com comprometimento cardiovascular do receptor — como insuficiência das valvas atrioventriculares e cardiomegalia — a avaliação ecocardiográfica fetal integra o planejamento cirúrgico.
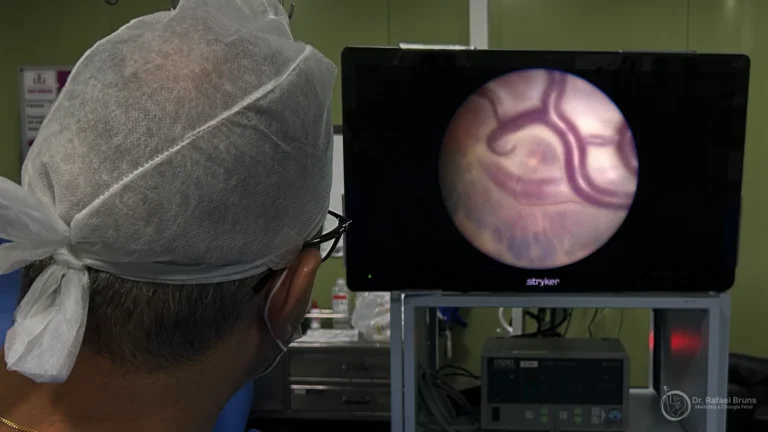
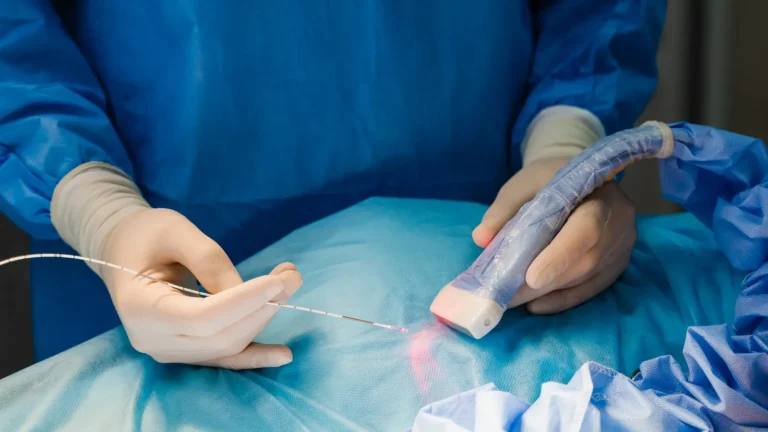
Como o procedimento funciona
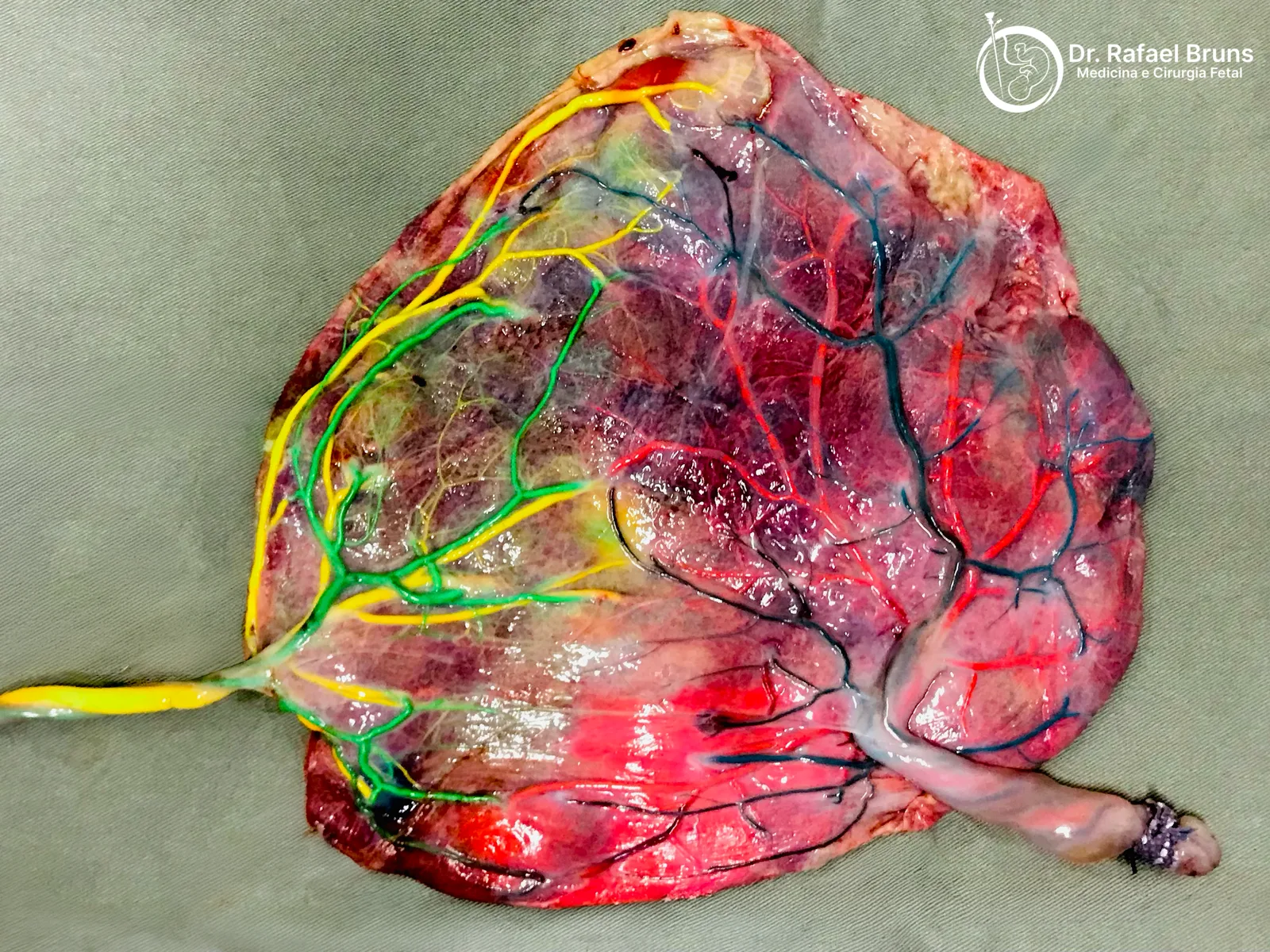
Por meio de uma pequena incisão no abdômen materno, o cirurgião fetal introduz um fetoscópio (uma câmera de fibra óptica de poucos milímetros) até a cavidade amniótica. O procedimento é realizado com anestesia local ou sedação leve, sem necessidade de anestesia geral para a mãe na maioria dos casos. A comunicação clara com a família sobre o que esperar antes, durante e após o procedimento é parte essencial do cuidado — o tempo cirúrgico médio é de 60 a 90 minutos e a internação costuma ser breve. Através do fetoscópio, visualiza diretamente a superfície da placenta e identifica as anastomoses vasculares — as conexões responsáveis pelo desequilíbrio de fluxo entre os gêmeos.
Com o laser, essas anastomoses são coaguladas uma a uma. O objetivo é separar funcionalmente as duas circulações fetais, eliminando a causa da doença — não apenas tratando suas consequências.
Técnica de Solomon
A técnica de Solomon, validada em ensaio clínico randomizado em 2014 (Slaghekke et al., Lancet), acrescentou um passo importante ao procedimento: após coagular cada anastomose individualmente, o cirurgião traça uma linha contínua de coagulação ao longo de todo o equador vascular da placenta. Isso reduz o risco de STFF recorrente e de sequência anemia-policitemia (TAPS), que podem ocorrer quando pequenas anastomoses residuais escapam à coagulação seletiva.
Por que o laser é diferente da amniodrenagem
A amniodrenagem (retirada do excesso de líquido amniótico) foi por muito tempo o único recurso disponível. Ela alivia os sintomas — reduz a pressão do polidrâmnio — mas não trata a causa. As anastomoses continuam ativas, o desequilíbrio persiste e o procedimento precisa ser repetido várias vezes. O laser, ao contrário, atua diretamente sobre a origem do problema.
Resultados do tratamento — o que os dados mostram
O estudo que estabeleceu definitivamente a superioridade do laser sobre a amniodrenagem foi o ensaio clínico randomizado publicado por Senat e colaboradores no New England Journal of Medicine em 2004. Foi o primeiro (e até hoje o principal) estudo randomizado comparando as duas abordagens na STFF grave. Os resultados foram tão expressivos que o estudo foi interrompido precocemente — o comitê de segurança considerou antiético continuar randomizando pacientes para amniodrenagem.
| Desfecho | Amniodrenagem | Laser fetoscópico |
|---|---|---|
| Como funciona | Remove excesso de líquido | Coagula anastomoses — elimina a causa |
| Sessões necessárias | Múltiplas (média 2,6) | Uma sessão (em geral) |
| Sobrevida ≥1 gemelar (6 meses) | 51% | 76% |
| Neurologia normal (6 meses) | 31% | 52% |
| Leucomalácia periventricular | 14% | 6% |
| Idade gestacional mediana ao parto | 29,0 semanas | 33,3 semanas |
| Disponibilidade | Ampla | Centros especializados |
Fonte: Senat MV et al. N Engl J Med. 2004;351:136-44.
Os números falam por si. A cirurgia a laser praticamente dobra a chance de desenvolvimento neurológico normal aos 6 meses (52% vs 31%), reduz pela metade a chance de lesão cerebral (leucomalácia periventricular de 6% vs 14%) e permite que os bebês permaneçam no útero por mais tempo — uma diferença mediana de mais de 4 semanas na idade gestacional ao parto. Em uma faixa de prematuridade em que cada semana a mais representa ganhos reais de maturidade pulmonar e neurológica, essa diferença é clinicamente muito significativa. Por esses resultados, a fetoscopia com ablação a laser das anastomoses placentárias é hoje considerada o padrão-ouro no tratamento da STFF grave — recomendada pelas principais diretrizes internacionais de medicina fetal. A redução do risco de leucomalácia periventricular (de 14% para 6%) é particularmente relevante: essa lesão cerebral está diretamente associada a sequelas neurológicas graves, incluindo paralisia cerebral, que afetam a qualidade de vida a longo prazo.
Acompanhamento pré-natal na gestação gemelar monocoriônica
Toda gestação gemelar monocoriônica — independentemente de apresentar ou não sinais de STFF — exige acompanhamento diferenciado. O protocolo recomendado inclui:
- Ultrassom a cada 2 semanas a partir de 16 semanas de gestação, com medida do maior bolsão de líquido amniótico na bolsa de cada um dos fetos
- Avaliação com Doppler da artéria umbilical e do ducto venoso quando indicado
- Monitoramento do crescimento fetal com atenção à discordância entre os gêmeos
- Avaliação da bexiga de ambos os fetos em cada exame
Esse acompanhamento rigoroso é o que permite identificar a STFF precocemente — muitas vezes ainda no estágio I — e encaminhar a gestante a um centro de referência a tempo de realizar o laser, quando indicado.
Mesmo após o tratamento a laser bem-sucedido, a prematuridade continua sendo um risco importante. A gestação monocoriônica tratada para STFF requer vigilância contínua até o parto, com atenção à possibilidade de recorrência, sequência anemia-policitemia (TAPS) e restrição de crescimento seletiva. A sequência anemia-policitemia pós-laser — também chamada TAPS (twin anemia-polycythemia sequence) — ocorre quando anastomoses vasculares residuais de pequeno calibre permanecem funcionantes após a coagulação. Nesse caso, há transferência lenta e contínua de sangue pelos vasos sanguíneos placentários remanescentes, sem os sinais clássicos de discrepância de líquido amniótico. O diagnóstico é feito pela avaliação Doppler da artéria cerebral média de ambos os fetos, que revela discrepância nos picos de velocidade sistólica.
Quando procurar avaliação urgente para STFF
- Polidrâmnio de início rápido em gestação gemelar
- Discrepância significativa de líquido amniótico entre as duas bolsas
- Bexiga do doador não visualizada no ultrassom
- Alterações no Doppler em gestação monocoriônica
- Diagnóstico ou suspeita de STFF em qualquer estágio
Na STFF, o timing importa. Quanto antes o encaminhamento ao especialista, mais opções terapêuticas.
A história da STFF — da descoberta ao laser
A história da síndrome da transfusão feto-fetal é a história de uma doença antiga que só recentemente passou a ter tratamento real. Conhecida há séculos, descrita formalmente no século XIX, ela permaneceu sem terapia efetiva até o final do século XX — e sem comprovação científica definitiva até 2004.
Das escrituras à ciência: os primeiros registros
O relato mais antigo que pode corresponder à STFF remonta à narrativa bíblica de Esaú e Jacó. Segundo o Gênesis, Esaú nasceu avermelhado e peludo, enquanto Jacó era pálido e menor. Ville (1997) e Berger (2000) sugeriram que essa descrição — dois gêmeos com características opostas ao nascimento — poderia ser compatível com a síndrome. É uma hipótese, naturalmente, mas ilustra o quão antiga pode ser essa condição.
Em 2000, Berger e colaboradores publicaram no Lancet um artigo identificando o que pode ser a primeira representação visual da STFF: a pintura holandesa De Wikkelkinderen (1617), que mostra dois recém-nascidos gêmeos com tamanhos e colorações claramente diferentes — um pletórico e outro pálido. A análise da obra, à luz do conhecimento médico atual, é consistente com transfusão feto-fetal.
Friedrich Schatz e a "terceira circulação"
O primeiro a descrever cientificamente o fenômeno foi o obstetra alemão Friedrich Schatz. Entre 1875 e 1886, Schatz estudou placentas de gestações gemelares e descreveu o que chamou de "terceira circulação" — um sistema de vasos que conectava os dois territórios fetais na placenta compartilhada. Sua publicação de 1886 no Archiv für Gynäkologie é considerada a descrição fundadora da doença.
Julian De Lia e o primeiro laser
Por mais de um século após Schatz, a STFF permaneceu sem tratamento específico. A amniodrenagem — retirada do excesso de líquido — aliviava os sintomas mas não impedia a progressão da doença. Em 1988, o cirurgião americano Julian De Lia realizou a primeira coagulação a laser das anastomoses placentárias por fetoscopia, desenvolvendo a técnica que viria a ser conhecida como FLOC (Fetoscopic Laser Occlusion of Chorioangiopagus vessels). Foi a primeira vez que se tentou eliminar a causa da doença, e não apenas suas consequências.
A consolidação europeia
Ao longo dos anos 1990, centros europeus refinaram e consolidaram a técnica. Yves Ville e Kypros Nicolaides em Londres, Kurt Hecher em Hamburgo — esses grupos acumularam casuísticas progressivamente maiores e demonstraram que o laser era viável, reprodutível e potencialmente superior à amniodrenagem. Ville e colaboradores publicaram em 1998 no British Journal of Obstetrics and Gynaecology resultados que reforçaram a viabilidade do método.
Em 1999, Rubén Quintero publicou seu sistema de estadiamento — os cinco estágios que organizam a gravidade da STFF e orientam a indicação cirúrgica. Esse sistema trouxe uma linguagem comum para descrever a doença e permitiu comparar resultados entre centros.
Senat 2004 — a prova definitiva
A evidência definitiva veio em 2004, com o estudo randomizado de Senat e colaboradores publicado no New England Journal of Medicine. Pela primeira vez, laser e amniodrenagem foram comparados em um ensaio clínico controlado. Os resultados foram tão favoráveis ao laser que o estudo foi interrompido antes do previsto — o comitê de ética considerou que não era justificável continuar oferecendo amniodrenagem como alternativa. A partir desse estudo, o laser se tornou o tratamento padrão para STFF grave em todo o mundo.
Solomon 2014 — o aperfeiçoamento da técnica
Em 2014, o grupo de Leiden (Slaghekke, Lopriore, Lewi e colaboradores, incluindo Dick Oepkes) publicou no Lancet o ensaio clínico que validou a técnica de Solomon — a coagulação contínua ao longo do equador vascular placentário, além da coagulação seletiva de cada anastomose. Esse refinamento reduziu as taxas de recorrência de STFF e de sequência anemia-policitemia pós-laser.
A história da STFF é a história de uma doença antiga que só recentemente passou a ter tratamento real. Na transfusão feto-fetal, tempo, diagnóstico correto e experiência da equipe fazem diferença concreta.
Uma história pessoal com a STFF
Meu primeiro contato com a síndrome da transfusão feto-fetal foi em 2001, durante a residência em ginecologia e obstetrícia. Uma paciente de 17 anos, acompanhada pelo Dr. Beduschi, chegou com diagnóstico de STFF grave. Os dois bebês não sobreviveram. Naquela época, o laser para STFF simplesmente não existia no Brasil. A única opção disponível era a amniodrenagem — que aliviava temporariamente os sintomas, mas não tratava a causa. Foi uma perda que marcou.
Carreguei esse caso por anos. A impotência diante de uma doença para a qual já existia tratamento em outros países — mas não aqui — foi determinante na minha trajetória.
Em outubro de 2015, tive a oportunidade de fazer o Advanced Course in Fetoscopic Laser Surgery no Leiden University Medical Center, na Holanda, sob orientação do Prof. Dick Oepkes — um dos maiores especialistas mundiais em cirurgia fetal a laser e coautor do estudo que validou a técnica de Solomon. Leiden é, historicamente, um dos centros de referência mundial em tratamento de STFF.
Do caso sem opção terapêutica em 2001 ao treinamento no centro que ajudou a desenvolver a técnica — essa trajetória resume, em escala pessoal, o que a medicina fetal conseguiu avançar em pouco mais de uma década.
Perguntas frequentes
Referências
- Schatz F. Eine besondere Art von einseitiger Polyhydramnie mit anderseitiger Oligohydramnie bei eineiigen Zwillingen. Arch Gynäkol. 1886;27:58-76.
- Berger HM, de Waard F, Molenaar Y. A case of twin-to-twin transfusion in 1617. Lancet. 2000;356:847-48.
- Quintero RA, Morales WJ, Allen MH, et al. Staging of twin-twin transfusion syndrome. J Perinatol. 1999;19:550-5.
- Senat MV, Deprest J, Boulvain M, et al. Endoscopic laser surgery versus serial amnioreduction for severe twin-to-twin transfusion syndrome. N Engl J Med. 2004;351:136-44.
- Slaghekke F, Lopriore E, Lewi L, et al. Fetoscopic laser coagulation of the vascular equator versus selective coagulation for twin-to-twin transfusion syndrome: an open-label randomised controlled trial. Lancet. 2014;383(9935):2144-51.
- Ville Y, Hecher K, Gagnon A, et al. Endoscopic laser coagulation in the management of severe twin-to-twin transfusion syndrome. Br J Obstet Gynaecol. 1998;105:446-53.
Médico especialista em Medicina Fetal, com atuação em Curitiba e Porto Alegre. Realiza cirurgia fetal, ultrassonografia especializada, procedimentos invasivos como amniocentese e biópsia de vilo corial, além do acompanhamento de gestações de alto risco.
RQE PR 12.169 · RQE PR 238
RQE RS 45.076 · RQE RS 45.079
Conteúdo com finalidade educativa. Não substitui avaliação médica individualizada. Diagnóstico e tratamento dependem de consulta presencial ou por telemedicina.