Cirurgia Fetal
Há uma pintura holandesa de 1617 que passou séculos num castelo perto de Amsterdam sem que ninguém soubesse o que mostrava. Dois bebês enrolados em cueiros brancos — um com o rosto vermelho, o outro branco como a neve. Em 2000, pesquisadores de Leiden descobriram o que o pintor havia registrado: as primeiras vítimas documentadas visualmente da transfusão feto-fetal.

O primeiro registro: Gênesis 25
“E quando chegaram os dias em que ela devia dar à luz, eis que havia gêmeos no seu ventre. E saiu o primeiro, todo vermelho como um manto de pelos; e chamaram o seu nome Esaú.”
— Gênesis 25, 24-25

Em 1979, o pediatra Philip Lanzkowsky publicou uma nota histórica no Pediatrics com uma observação direta: um recém-nascido gemelar descrito como “todo vermelho” é uma descrição precisa de policitemia neonatal — excesso de glóbulos vermelhos no sangue. E a principal causa de policitemia em gêmeos monozigóticos é exatamente a transfusão feto-fetal. O feto receptor recebe sangue em excesso, fica hipervolêmico, seu hematócrito dispara, e ao nascer apresenta a coloração avermelhada que a Bíblia descreve com precisão clínica acidental.
Jacó, que nasceu logo depois, pálido e menor, seria o feto doador — anêmico, hipovolêmico, com crescimento restrito.
A hipótese tem limitações. As diferenças de personalidade entre os irmãos na vida adulta — Esaú, o caçador impetuoso; Jacó, o homem contemplativo das tendas — sugerem para alguns estudiosos que eram dizigóticos, e portanto sem risco de STFF. Mas Lanzkowsky foi além: especulou que as possíveis restrições intelectuais de Esaú poderiam ser sequelas de lesão cerebral por hiperviscosidade sanguínea — uma das complicações neurológicas da policitemia neonatal.
Quase duas décadas depois, Yves Ville — um dos pioneiros do laser fetal, escrevendo de Londres em 1997 — abriu seu influente editorial sobre gestação gemelar monocoriônica exatamente com essa cena. Ele observou que se Rebeca tivesse tido acesso ao ultrassom no primeiro trimestre, boa parte da controvérsia sobre o tipo de gemelaridade de Esaú e Jacó — e sobre a possibilidade de transfusão feto-fetal — talvez nunca tivesse existido (Ville, Ultrasound Obstet Gynecol 1997).
É uma hipótese sobre o Gênesis. Mas é uma hipótese que qualquer neonatologista reconheceria como clinicamente plausível.
1617: os bebês do castelo
Numa manhã de abril de 1617, no bairro nobre de Amsterdam, a esposa do prefeito Jacob de Graeff deu à luz gêmeos. Os registros genealógicos da família não os mencionam — sinal quase certo de que morreram no dia do nascimento, ou pouco depois. Alguém — um pintor anônimo da escola holandesa — foi chamado para imortalizá-los antes que fossem enterrados. A prática de retratar crianças mortas era comum no século XVII, e os bebês eram frequentemente pintados com os olhos abertos para indicar que haviam nascido vivos.
O quadro que resultou desse encontro — De Wikkelkinderen, “As Crianças Enroladas” — passou séculos viajando entre castelos e museus holandeses sem despertar atenção clínica. Até que em 2000, H.M. Berger e colaboradores do Leiden University Medical Centre olharam para ele com olhos de médicos.
O que viram: dois recém-nascidos do mesmo tamanho, um com o rosto intensamente vermelho, o outro com o rosto branco. A diferença de coloração era tão marcante que o artista a reproduziu com precisão — e foi tão hábil que a luz refletida do rosto pálido ilumina até o tecido do cueiro ao redor. O diagnóstico proposto no Lancet: transfusão feto-fetal (Berger et al., 2000).

Por que provavelmente é TAPS, não STFF clássica
Aqui entra uma observação que os próprios autores de 2000 não podiam fazer — porque o TAPS como entidade clínica distinta só seria formalmente descrito sete anos depois.
Na STFF clássica, o desequilíbrio hemodinâmico é intenso e progressivo: o doador cresce pouco, o receptor torna-se macrossômico. Os bebês chegam ao parto com tamanhos frequentemente discordantes. Nos estágios avançados, morrem com hidropisia. A sobrevivência de ambos após nascimento liveborn em estágios graves é incomum sem tratamento.
O quadro de 1617 mostra bebês do mesmo tamanho — detalhe que o próprio Berger registra no artigo e que usa para argumentar que a transfusão teria ocorrido de forma aguda perto do parto.
Mas há uma explicação mais precisa, apoiada pelos critérios diagnósticos formalizados por Slaghekke e colaboradores do mesmo Leiden em 2010: a sequência anemia-policitemia gemelar — TAPS, twin anemia-polycythemia sequence. O TAPS é causado por anastomoses placentárias de calibre muito pequeno, com menos de 1 mm de diâmetro. Essas anastomoses permitem uma transfusão lenta: apenas 5 a 15 mL de sangue por 24 horas — suficientes para criar uma discordância de hemoglobina superior a 8 g/dL entre os gêmeos, mas insuficientes para causar a discordância de líquido amniótico ou o desequilíbrio de crescimento típicos da STFF clássica. Os bebês nascem do mesmo tamanho. Mas com colorações opostas (Slaghekke et al., Fetal Diagn Ther 2010).
É exatamente esse o padrão do quadro de 1617.
Os bebês De Graeff provavelmente morreram de anemia grave num e policitemia com hiperviscosidade no outro. Não de STFF clássica — mas de uma condição que a medicina do século XXI chama de TAPS.
1875–1886: Friedrich Schatz e a terceira circulação
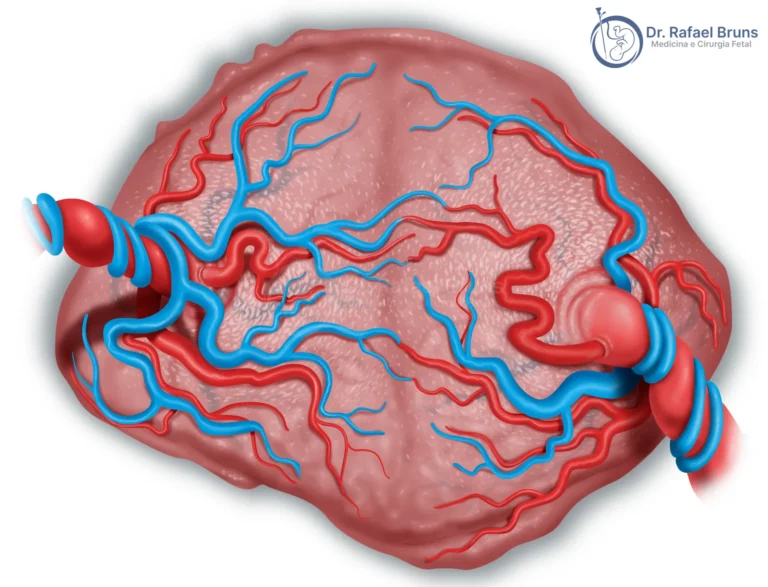
O médico alemão Friedrich Schatz foi o primeiro cientista a entender o mecanismo. Em 1875 e depois em 1886, após estudar dezenas de placentas gemelares injetando soluções coloradas nos vasos, descreveu o que chamou de “terceira circulação”: um sistema de conexões vasculares entre os territórios dos dois fetos na placenta compartilhada.
Num de seus casos, observou exatamente o que a medicina moderna reconhece como STFF grave: um gêmeo edemaciado, com bexiga distendida e poliúria; o outro, atrofiado, com bexiga vazia. O receptor morreu em 12 horas. O doador, o stuck twin, em 53 horas. Schatz compreendeu que a causa estava nas conexões vasculares — na “terceira circulação” que ele havia descoberto (Glennon et al., Twin Res Hum Genet 2016).
A doença tinha descrição científica. Faltava tratamento.
1988: o primeiro laser
Por cem anos, a STFF permaneceu sem terapia específica. A única opção era a amniodrenagem — retirada do excesso de líquido amniótico do receptor — que aliviava temporariamente os sintomas mas não tocava nas anastomoses. A mortalidade permanecia de 70 a 100% nos casos graves.
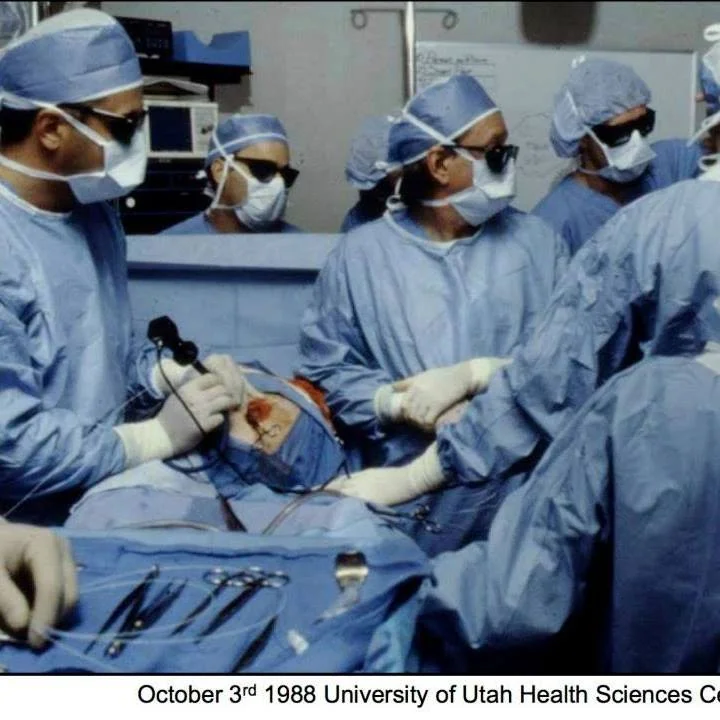
Em 3 de outubro de 1988, o obstetra americano Julian De Lia realizou no University of Utah Health Sciences Center a primeira coagulação a laser das anastomoses placentárias em um ser humano. O procedimento havia sido testado antes em ovelhas e macacos rhesus. Naquele dia, foi aplicado numa paciente transferida de Montana com STFF grave — o único tratamento disponível era a compaixão.
Os gêmeos nasceram 8 semanas depois, com 27 semanas de gestação. Ambos sobreviveram (De Lia e Kuhlmann, Am J Perinatol 2014).
Sete anos depois, em 1995, Yves Ville, Kypros Nicolaides e colaboradores do King’s College em Londres publicaram no New England Journal of Medicine uma série de casos tratados com laser — a revista de maior impacto do mundo. O artigo do NEJM foi o que popularizou internacionalmente o procedimento e levou a técnica a centros ao redor do globo. Em documentários e na memória coletiva da especialidade, a publicação no NEJM às vezes é confundida com a origem do método. A história é outra: De Lia veio primeiro. O NEJM veio depois, e foi o que tornou o laser conhecido.
2001: um caso que não saiu da memória
Há casos que ficam. Em 2001, durante a residência em ginecologia e obstetrícia, acompanhei uma paciente de 17 anos com diagnóstico de STFF grave. Os dois bebês não sobreviveram. Naquela época, o laser simplesmente não existia no Brasil. A única opção disponível era a amniodrenagem — que aliviava temporariamente, mas não tratava a causa. A impotência diante de uma doença para a qual já existia tratamento em outros países foi determinante na minha trajetória.
1999: a linguagem comum
Enquanto os centros europeus acumulavam experiência com o laser, faltava uma forma padronizada de descrever a gravidade da doença. Em 1999, Rubén Quintero e colaboradores publicaram no Journal of Perinatology a classificação de Quintero — um sistema de cinco estágios progressivos baseados em achados ultrassonográficos. Pela primeira vez, médicos de diferentes centros podiam descrever a mesma doença com os mesmos critérios. O estadiamento de Quintero virou a referência mundial para estratificar a STFF e orientar a indicação do laser — função que mantém até hoje.
2004: a prova definitiva
Em 2004, Marie-Victoire Senat e colaboradores publicaram no New England Journal of Medicine o ensaio clínico randomizado que estabeleceu definitivamente a superioridade do laser sobre a amniodrenagem. Os resultados foram tão expressivos que o estudo foi interrompido antes do previsto — o comitê de ética considerou antiético continuar randomizando pacientes para amniodrenagem.
Sobrevida de ao menos um gemelar: 76% com laser, 51% com amniodrenagem. Desenvolvimento neurológico normal aos 6 meses: 52% com laser, 31% com amniodrenagem. O laser tornou-se o tratamento padrão mundial (Senat et al., N Engl J Med 2004).
O efeito colateral inesperado
A medicina raramente resolve um problema sem criar outro.
Com o laser como tratamento padrão, os centros de cirurgia fetal passaram a tratar centenas de casos por ano. E algo inesperado começou a aparecer nos dados: uma complicação que antes era raríssima tornou-se relativamente frequente. Em 2007, pesquisadores do Leiden University Medical Centre — liderados por Enrico Lopriore e Dick Oepkes — descreveram formalmente dois casos de gêmeos monocoriônicos com discordância extrema de hemoglobina mas sem qualquer discordância de líquido amniótico. Os bebês tinham o mesmo tamanho. Mas um estava gravemente anêmico e o outro, policitêmico. Chamaram essa condição de TAPS — sequência anemia-policitemia gemelar (Lopriore et al., Placenta 2007).
O mecanismo estava nas anastomoses residuais. Nas placentas monocoriônicas, as conexões vasculares variam em calibre. As maiores são identificadas e coaguladas durante a fetoscopia. Mas as muito pequenas — menos de 1 mm de diâmetro — frequentemente escapam à visualização direta. Essas anastomoses minúsculas não são grandes o suficiente para causar a STFF clássica com seu desequilíbrio agudo de volume. Mas são funcionantes. E funcionando lentamente, criam transfusão crônica de hemoglobina — sem discordância de líquido amniótico, sem discordância de tamanho — exatamente o padrão que os bebês De Graeff provavelmente apresentaram em 1617.
O laser que curou a STFF havia inadvertidamente aumentado a incidência do TAPS. No centro de Leiden, a incidência de TAPS pós-laser chegou a 8% dos casos tratados. Em outros centros, os dados variaram entre 2% e 13%, dependendo dos critérios e da completude do seguimento (Slaghekke et al., Fetal Diagn Ther 2010).
- Qualquer gestação gemelar monocoriônica precisa de ultrassom a cada 2 semanas a partir de 16 semanas
- Discordância de líquido amniótico entre as bolsas — sinal de alerta para STFF
- Discordância de velocidade de pico sistólico na artéria cerebral média sem discordância de líquido — padrão típico de TAPS
- Diagnóstico de STFF ou TAPS em qualquer estágio: encaminhar imediatamente a centro especializado
2014: a técnica de Solomon fecha o círculo

A solução veio do mesmo grupo de Leiden que havia identificado o quadro de 1617 como um possível caso histórico de transfusão feto-fetal.
Femke Slaghekke, Enrico Lopriore, Dick Oepkes e colaboradores desenvolveram uma modificação técnica do laser: além de coagular cada anastomose individualmente, o cirurgião traça uma linha contínua de ablação ao longo de todo o equador vascular da placenta — fechando também as anastomoses periféricas pequenas que escapavam à coagulação seletiva.
O Prof. Dick Oepkes, um dos criadores da técnica, contou essa história durante o treinamento em cirurgia fetal a laser que realizei em Leiden em outubro de 2015: o nome “Solomon” é uma referência direta ao Rei Salomão — o monarca bíblico que, diante de duas mães disputando o mesmo filho, ameaçou dividir a criança ao meio para revelar a verdade. Na técnica, a linha de laser divide a circulação placentária ao meio — na tentativa de salvar os dois bebês.


O ensaio clínico randomizado publicado no Lancet em 2014 validou a abordagem com números que falam por si: no grupo com laser seletivo padrão, 16% dos casos desenvolveram TAPS pós-laser e 7% tiveram STFF recorrente — totalizando 21% de complicações por anastomoses residuais. Com a técnica de Solomon, o TAPS caiu para 3% e a STFF recorrente para 1% — totalizando apenas 4% de complicações residuais. A linha contínua de coagulação fechava exatamente as anastomoses periféricas minúsculas que o laser seletivo deixava abertas (Slaghekke et al., Lancet 2014).
O círculo que se fecha
Há uma ironia histórica que só se torna visível quando os fatos são colocados em sequência.
Os bebês De Graeff morreram em 7 de abril de 1617, provavelmente de uma condição causada por anastomoses placentárias muito pequenas — o que hoje chamamos de TAPS. Quatro séculos depois, o tratamento criado para a STFF clássica produziu inadvertidamente mais casos dessa mesma condição. E a solução para esse problema foi desenvolvida exatamente em Leiden — a mesma cidade que havia identificado o quadro de 1617 como possível registro histórico da doença.
O Rei Salomão, que deu nome à técnica, aparece também no fio bíblico que começa com Esaú e Jacó. A medicina fetal moderna, sem perceber, construiu uma narrativa que conecta o Gênesis ao Leiden University Medical Centre em linha quase direta.
E os bebês do castelo — cujos registros familiares não sobreviveram, cujos nomes não conhecemos — tornaram-se parte dessa história graças ao olhar de um pintor anônimo que decidiu retratar com precisão o que via: dois recém-nascidos do mesmo tamanho, um vermelho, um branco, enrolados em cueiros brancos para nunca mais acordar.
Perguntas frequentes
Referências
- Lanzkowsky P. Twin-to-twin transfusion — an historic note. Pediatrics. 1979;64(3):309.
- Ville Y. Monochorionic twin pregnancies: “les liaisons dangereuses”. Ultrasound Obstet Gynecol. 1997;10:82–85.
- Berger HM, de Waard F, Molenaar Y. A case of twin-to-twin transfusion in 1617. Lancet. 2000;356:847–48.
- Corsello G. Twins among history, myth and arts. J Matern Fetal Neonatal Med. 2013;26(S2):5–6.
- De Lia JE, Kuhlmann RS. Twin-to-twin transfusion syndrome — 30 years at the front. Am J Perinatol. 2014;31:S7–S12.
- Glennon CL et al. The history of treatment of twin-to-twin transfusion syndrome. Twin Res Hum Genet. 2016;19(3):168–174.
- Lopriore E et al. Twin anemia-polycythemia sequence in two monochorionic twin pairs without oligo-polyhydramnios sequence. Placenta. 2007;28:47–51.
- Senat MV et al. Endoscopic laser surgery versus serial amnioreduction for severe twin-to-twin transfusion syndrome. N Engl J Med. 2004;351:136–44.
- Slaghekke F et al. Twin anemia-polycythemia sequence: diagnostic criteria, classification, perinatal management and outcome. Fetal Diagn Ther. 2010;27(4):181–190.
- Slaghekke F et al. Fetoscopic laser coagulation of the vascular equator versus selective coagulation for twin-to-twin transfusion syndrome (SOLOMON trial). Lancet. 2014;383(9935):2144–51.
- Ville Y, Hyett J, Hecher K, Nicolaides K. Preliminary experience with endoscopic laser surgery for severe twin-twin transfusion syndrome. N Engl J Med. 1995;332:224–7.
Conteúdo com finalidade histórica e educativa. Não substitui avaliação médica individualizada. Diagnóstico e tratamento dependem de consulta presencial ou por telemedicina.