MEDICINA FETAL · CIRURGIA FETAL
Hérnia Diafragmática Congênita (HDC): diagnóstico pré-natal, prognóstico e tratamento
A hérnia diafragmática congênita é uma malformação em que um defeito no diafragma permite que órgãos abdominais migrem para o tórax do bebê, comprometendo o desenvolvimento dos pulmões. O diagnóstico pré-natal é essencial para estimar gravidade, planejar o nascimento e, em casos selecionados, discutir tratamento fetal.
Em resumo
- A gravidade da HDC não está no "buraco no diafragma" — está no impacto sobre o desenvolvimento pulmonar (hipoplasia pulmonar e hipertensão pulmonar)
- O diagnóstico costuma ser feito no ultrassom morfológico, por volta de 20 semanas
- Em casos graves e selecionados, existe a possibilidade de tratamento fetal (FETO) — o ensaio TOTAL (NEJM 2021) demonstrou aumento de sobrevida de 15% para 40%
- O planejamento do parto em centro experiente muda o desfecho — mesmo quando não há indicação de intervenção fetal
O que é a hérnia diafragmática congênita
A hérnia diafragmática congênita (HDC) é uma malformação em que existe um defeito no diafragma — o músculo que separa o tórax do abdômen. Por causa dessa abertura, órgãos da cavidade abdominal, como intestino, estômago e, em casos mais graves, o fígado, podem migrar para dentro da cavidade torácica do bebê durante a gestação.
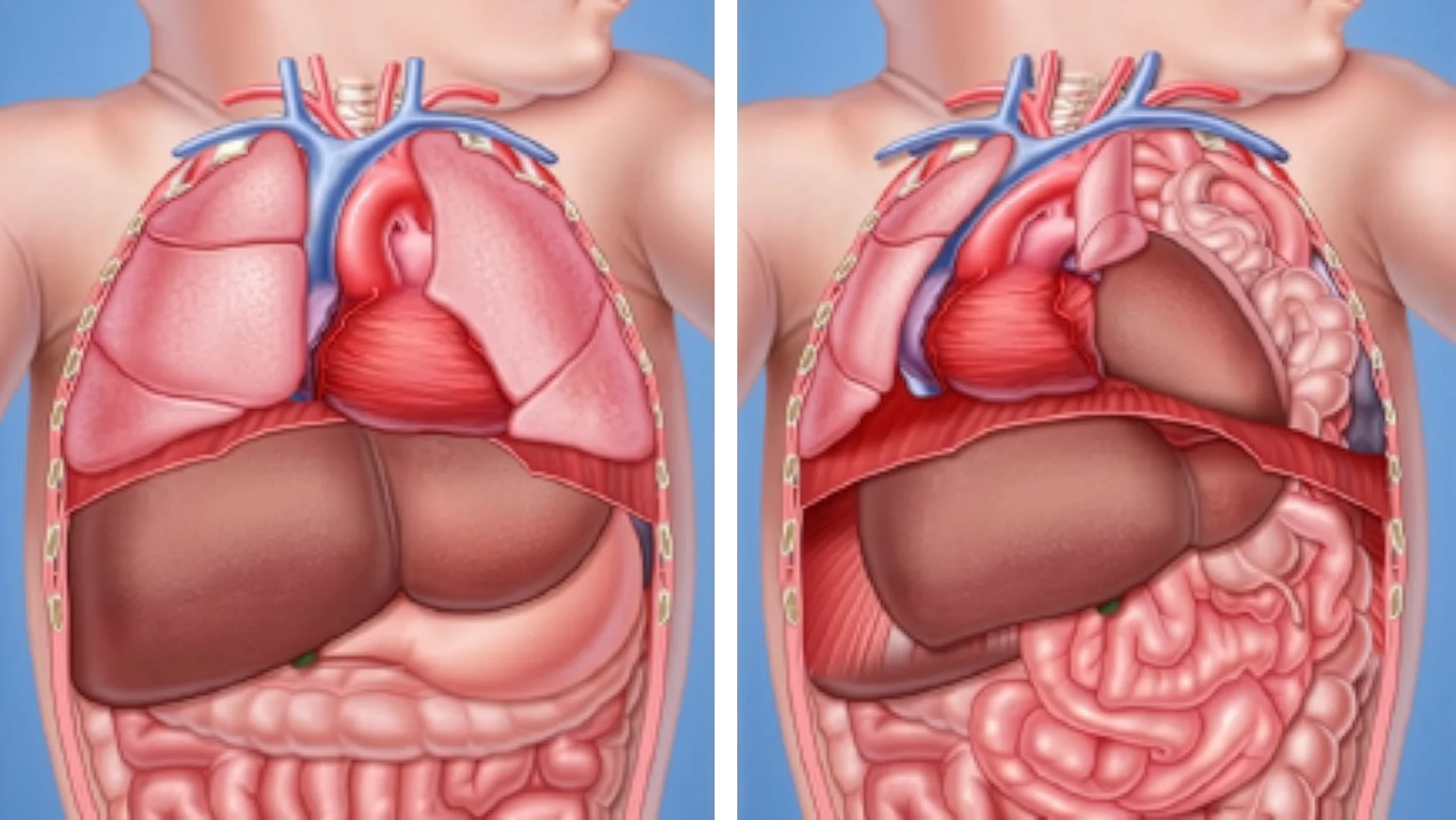
O resultado dessa herniação é que os pulmões perdem espaço para crescer e se desenvolvem de forma insuficiente. Esse é o núcleo do problema: não é apenas um "buraco no músculo" — é o que essa abertura faz com o desenvolvimento pulmonar que define a gravidade da HDC.
Como a HDC acontece durante a formação do diafragma
O diafragma se forma nas primeiras semanas de gestação, entre a 8ª e a 10ª semana. Quando essa formação ocorre de forma incompleta, surge o defeito que caracteriza a hérnia diafragmática congênita. A maior parte dos casos ocorre no lado esquerdo — onde a barreira natural é menos robusta. Casos do lado direito também existem, e casos bilaterais, embora raros, costumam ter prognóstico mais reservado.
A hérnia diafragmática congênita não é hereditária na maioria dos casos. Mas em uma parcela dos pacientes podem estar presentes alterações genéticas ou cromossômicas que influenciam diretamente o prognóstico, o que torna a investigação genética parte importante da avaliação.
Por que a HDC pode ser uma doença grave
A gravidade da hérnia diafragmática não está apenas no defeito anatômico. O que torna a HDC potencialmente fatal é o seu impacto sobre os pulmões e sobre a circulação pulmonar.
Quando as vísceras ocupam o tórax durante a gestação, o espaço disponível para os pulmões crescerem é reduzido. Os pulmões do bebê podem nascer pequenos — condição chamada de hipoplasia pulmonar — e com vasos sanguíneos anormalmente desenvolvidos. Esse conjunto explica por que muitos bebês com HDC apresentam dificuldade respiratória grave logo após o nascimento, antes mesmo de qualquer cirurgia ser feita.
Hipoplasia pulmonar e hipertensão pulmonar: o centro do problema
Dois termos médicos aparecem repetidamente quando se fala em hérnia diafragmática congênita: hipoplasia pulmonar e hipertensão pulmonar.
A hipoplasia pulmonar é o crescimento insuficiente dos pulmões. Os pulmões pequenos têm menos capacidade de oxigenar o sangue, o que gera crise respiratória logo ao nascimento.
A hipertensão pulmonar é uma alteração nos vasos sanguíneos dos pulmões que, mesmo quando os pulmões crescem melhor com o tempo, pode persistir e comprometer a circulação. É uma das principais causas de instabilidade grave nas primeiras horas e dias de vida do recém-nascido com HDC.
Esses dois componentes — e não apenas o defeito no diafragma — são o que os médicos precisam avaliar antes, durante e depois do nascimento.
Como o ultrassom no pré-natal faz o diagnóstico
O diagnóstico pré-natal da hérnia diafragmática congênita costuma ser feito pela primeira vez no ultrassom morfológico, em geral por volta de 20 semanas de gestação.
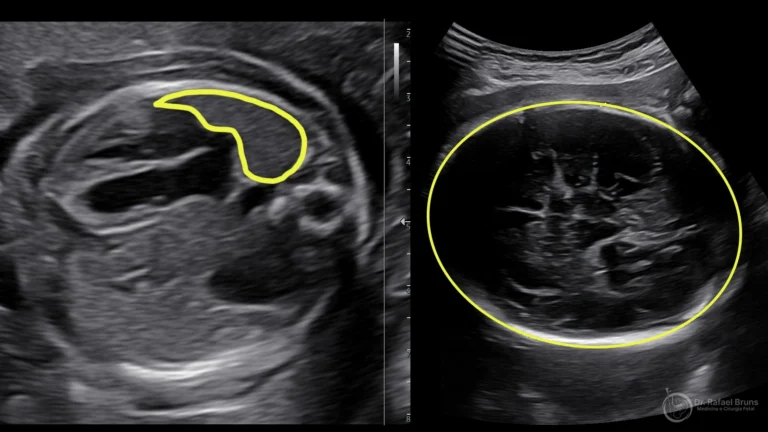
No exame, o médico pode observar:
- Estômago ou alças intestinais dentro do tórax do bebê
- Desvio do coração para o lado oposto à hérnia
- Ausência ou redução do volume pulmonar visível
- Posição do fígado dentro do tórax em casos mais graves
- Polidrâmnio em alguns casos
O diagnóstico pré-natal não serve apenas para "nomear a doença". Ele é o ponto de partida para estimar gravidade, investigar condições associadas e — muito importante — planejar onde e como o bebê deve nascer.
O que a ressonância magnética fetal pode acrescentar
Quando a hérnia diafragmática é diagnosticada no ultrassom, a ressonância magnética fetal pode ser solicitada como complemento. Ela oferece algumas vantagens que o ultrassom, por si só, não consegue entregar com a mesma precisão:
- Medida mais acurada do volume pulmonar fetal
- Avaliação precisa de quanto do fígado está herniado
- Melhor caracterização da anatomia em casos de difícil visualização ultrassonográfica
- Informações que complementam a estratificação de risco
A ressonância magnética não substitui o ultrassom — ela acrescenta informação clínica relevante em casos em que há dúvida diagnóstica ou necessidade de planejamento mais detalhado.
Como avaliamos a gravidade ainda durante a gestação
Nem toda hérnia diafragmática congênita tem o mesmo prognóstico. A gravidade varia de casos mais leves, em que o bebê pode se sair bem com cuidados neonatais adequados, até casos severos, com risco muito elevado de mortalidade.
Os principais fatores que orientam a avaliação de gravidade são:
Relação pulmão-cabeça (LHR): uma medida obtida no ultrassom que compara o tamanho do pulmão contralateral com a circunferência da cabeça do bebê. Uma LHR abaixo de 1,0 é um dos critérios que indica caso grave, com maior risco e potencial candidatura para discussão de tratamento fetal.
Posição do fígado: quando o fígado hernia para dentro do tórax ("liver up"), o prognóstico se torna significativamente mais reservado.
Lado da hérnia: casos à esquerda são mais frequentes; casos à direita, embora menos comuns, costumam ser mais graves dado que o fígado está invariavelmente envolvido.
Anomalias associadas: a presença de cardiopatias ou alterações genéticas influencia diretamente o prognóstico e a tomada de decisão.
Essa estratificação é o que permite individualizar o cuidado — e é onde a medicina fetal especializada faz diferença real.
Quando a FETO pode ser considerada
Em casos selecionados de hérnia diafragmática congênita com hipoplasia pulmonar grave, existe a possibilidade de tratamento ainda durante a gestação: a oclusão traqueal endoluminal fetoscópica (FETO).
O procedimento consiste em introduzir, por via fetoscópica, um pequeno balão dentro da traqueia do bebê ainda no útero. Com a traqueia ocluída, o líquido que os pulmões normalmente produzem fica retido, aumentando a pressão intrapulmonar e estimulando o crescimento pulmonar. O balão é retirado antes do nascimento — geralmente em torno de 34 semanas —, permitindo que os pulmões completem a maturação. Para entender melhor o procedimento, veja também o artigo sobre balão traqueal fetal: como funciona a FETO, quando ela pode ser indicada e por que o balão precisa ser retirado antes do parto.
A FETO não é indicada para todos os casos. Os critérios de seleção são rigorosos: o maior benefício documentado se aplica a fetos com HDC esquerda isolada e hipoplasia pulmonar grave — justamente o grupo com pior prognóstico sem intervenção. O ensaio clínico randomizado TOTAL, publicado no New England Journal of Medicine em 2021, demonstrou melhora significativa na sobrevida nos casos graves (40% de sobrevida com FETO versus 15% sem intervenção).
Riscos do procedimento que precisam ser discutidos com cada família incluem risco aumentado de ruptura prematura de membranas e parto prematuro. Por isso, após a colocação do balão, é necessário que a gestante permaneça próxima ao centro de referência até o nascimento.
Quando procurar avaliação especializada
- Diagnóstico de HDC no ultrassom morfológico ou em qualquer exame de imagem
- Dúvida sobre a gravidade do caso ou sobre a necessidade de intervenção fetal
- Laudos contraditórios ou avaliação de gravidade inconclusiva
- Necessidade de planejar onde e como o bebê deve nascer
- Interesse em discutir elegibilidade para FETO em caso grave
Uma breve história da cirurgia fetal para HDC
O caminho até o FETO moderno levou décadas — e passou por erros importantes que refinaram o que sabemos hoje.
Linha do tempo — marcos na história da cirurgia fetal para hérnia diafragmática congênita
Michael Harrison (UCSF) realiza as primeiras tentativas de correção do defeito diafragmático por histerotomia aberta. Os resultados são decepcionantes — a descoberta mais importante é que corrigir o diafragma não resolve a hipoplasia pulmonar já estabelecida.
A virada conceitual: experimentos em animais demonstram que bloquear a traqueia faz os pulmões crescerem. A pressão intraluminal do líquido retido estimula proliferação celular. Nasce o conceito de plug-unplug.
Harrison realiza as primeiras oclusões traqueais em humanos com clipe no pescoço fetal, ainda por histerotomia aberta. Os resultados são mistos.
Jan Deprest (Leuven, Bélgica) desenvolve a abordagem percutânea com fetoscópio, substituindo a histerotomia por uma pequena incisão e introduzindo o balão por via endoscópica. O risco materno cai substancialmente — essa é a base do procedimento FETO atual.
Primeiro ensaio clínico randomizado — resultado negativo. O estudo não demonstra diferença de sobrevida, mas a crítica metodológica mostra grupos heterogêneos e critérios insuficientemente rigorosos. A técnica continua sendo desenvolvida na Europa.
Consolidação em Leuven. Deprest e colaboradores estabelecem o o/e LHR e a posição hepática como parâmetros de seleção. A FETO passa de "experimental" para procedimento com protocolo definido em centros de alto volume.
Dr. Rafael Bruns e Dr. André Bradley realizam a primeira cirurgia fetal (FETO) para hérnia diafragmática congênita do serviço. A técnica passa a integrar a avaliação em casos selecionados de HDC com LHR abaixo de 1,0.
TOTAL Trial publicado no New England Journal of Medicine. Resultado definitivo para casos graves: FETO aumenta a sobrevida de 15% para 40%. O editorial de Cole enquadra o TOTAL como marco que transformou a prática em evidência nível I.
Era pós-TOTAL. A reanálise dos dados sugere que o timing do procedimento — idealmente antes de 30 semanas — importa mais que a classificação de gravidade isolada. O SMART-TO, um balão com deflação não-invasiva por ressonância magnética, entra em trials clínicos — se validado, eliminará a necessidade da segunda intervenção.
Como o parto e o nascimento devem ser planejados
O planejamento do parto em casos de hérnia diafragmática congênita é parte essencial do tratamento. Não se trata apenas de escolher "onde dar à luz" — trata-se de garantir que o recém-nascido terá acesso imediato à equipe e à estrutura necessárias.
O nascimento deve ocorrer em um centro com experiência em HDC, que disponha de UTI neonatal de alta complexidade, cirurgia pediátrica, cardiologia pediátrica e equipe treinada para estabilização de recém-nascidos com dificuldade respiratória grave.
O diagnóstico pré-natal, além de informar, permite organizar esse caminho com antecedência — e isso, por si só, muda o desfecho.
O que acontece com o bebê após o nascimento
Ao nascer, o bebê com hérnia diafragmática congênita pode apresentar dificuldade respiratória importante, dependendo da gravidade da hipoplasia pulmonar. Isso exige resposta rápida e especializada.
O manejo neonatal inicial inclui:
- Intubação precoce em casos indicados
- Evitar ventilação com máscara e balão, que pode distender o estômago e agravar a compressão pulmonar
- Sonda nasogástrica para descompressão gástrica
- Ventilação mecânica protetora
- Suporte farmacológico para hipertensão pulmonar
- Monitorização intensiva da circulação
A estabilização clínica precede a cirurgia. O recém-nascido não vai direto para o centro cirúrgico — primeiro a equipe precisa garantir que o bebê esteja estável o suficiente para tolerar a intervenção.
Quando a cirurgia neonatal é feita
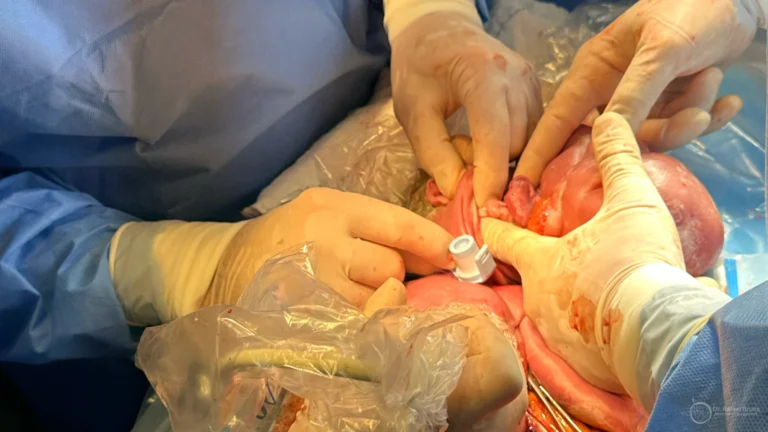
A cirurgia pediátrica na HDC tem como objetivo reposicionar as vísceras de volta para a cavidade abdominal e reparar o defeito no diafragma, com sutura direta ou, quando necessário, com uso de um patch.
A cirurgia é fundamental — mas ela não resolve o componente pulmonar da doença. Pulmões pequenos não se tornam normais imediatamente após a correção do defeito diafragmático. O crescimento pulmonar após a cirurgia acontece ao longo dos primeiros anos de vida, e parte das crianças com HDC grave continuará precisando de suporte respiratório por semanas ou meses após a correção.
Qualidade de vida e seguimento a longo prazo
A HDC não termina com a alta hospitalar. Muitas crianças evoluem muito bem, especialmente as de apresentação menos grave. Mas parte dos sobreviventes, sobretudo de casos severos, pode necessitar de acompanhamento prolongado por:
- Dificuldades respiratórias persistentes e uso de broncodilatadores
- Hipertensão pulmonar residual
- Refluxo gastroesofágico e dificuldades alimentares
- Atraso de crescimento
- Questões de neurodesenvolvimento
A qualidade de vida das crianças com HDC depende muito da gravidade inicial, do suporte recebido nas primeiras semanas e da qualidade do seguimento depois. Uma equipe multidisciplinar — neonatologia, pneumologia, cirurgia, gastroenterologia, neurologia e fisioterapia — é o modelo de cuidado que melhor serve a essa população.
Risco de recorrência em outra gestação
O risco de que a hérnia diafragmática congênita se repita em outra gestação é baixo — estimado em torno de 2% quando não há síndrome genética identificada. Quando há causa genética documentada, o risco pode ser maior e deve ser avaliado caso a caso com aconselhamento genético antes de uma nova gravidez.
Quando buscar uma segunda opinião
- O diagnóstico gerou dúvida ou os laudos são contraditórios
- Você quer entender melhor a gravidade do caso e o que esperar
- Foi orientada a considerar FETO e quer avaliar com outro especialista
- Precisa de orientação sobre onde e como planejar o parto
Perguntas frequentes sobre hérnia diafragmática congênita
Referências
- Deprest JA, Nicolaides KH, Benachi A, et al. Randomized trial of fetal surgery for severe left diaphragmatic hernia. N Engl J Med. 2021;385(2):107-118. (TOTAL Trial — casos graves)
- Deprest JA, Benachi A, Gratacos E, et al. Randomized trial of fetal surgery for moderate left diaphragmatic hernia. N Engl J Med. 2021;385(2):119-129. (TOTAL Trial — casos moderados)
- Harrison MR, Adzick NS, Flake AW, et al. Correction of congenital diaphragmatic hernia in utero: VI. Hard-earned lessons. J Pediatr Surg. 1993;28(10):1411-1418.
- Jani JC, Nicolaides KH, Gratacós E, et al. Severe diaphragmatic hernia treated by fetal endoscopic tracheal occlusion. Ultrasound Obstet Gynecol. 2009;34(3):304-310.
- Congenital Diaphragmatic Hernia Study Group. Estimating disease severity of congenital diaphragmatic hernia in the first 5 minutes of life. J Pediatr Surg. 2001;36(1):141-145.
Médico especialista em Medicina Fetal, com atuação em Curitiba e Porto Alegre. Realiza cirurgia fetal, ultrassonografia especializada, procedimentos invasivos como amniocentese e biópsia de vilo corial, além do acompanhamento de gestações de alto risco.
RQE PR 12.169 · RQE PR 238
RQE RS 45.076 · RQE RS 45.079
Conteúdo com finalidade educativa. Não substitui avaliação médica individualizada. Diagnóstico e tratamento dependem de consulta presencial ou por telemedicina.