Anemia Fetal · História da Medicina
Por milênios, médicos observavam bebês que nasciam com a pele amarelada, o corpo inchado de líquido, e morriam nos primeiros dias. Hipócrates descreveu o quadro. Nenhum dos dois entendeu o que causava. A resposta levaria séculos — e quando veio, resultaria em uma das maiores vitórias da medicina preventiva da história.

O mistério que durou milênios
No século V a.C., Hipócrates de Cós — considerado o pai da medicina — registrou o caso de um bebê que nasceu inchado, com a pele amarelada, e morreu logo após o parto. O quadro tinha um nome — hidropsia — mas não tinha explicação.
Durante os dois mil anos seguintes, a mesma cena se repetiu em partos em toda a Europa, Ásia e Américas. Bebês morriam de uma doença que os médicos reconheciam mas não compreendiam. Às vezes acontecia na primeira gestação, mas era mais comum nas seguintes. Às vezes afetava um filho, às vezes vários. A mãe ficava bem. O bebê não.
A doença tinha muitas faces: alguns bebês nasciam com icterícia grave — o amarelo da bilirrubina se acumulando nos tecidos. Outros com anemia tão profunda que o coração não conseguia sustentar a circulação. Os casos mais graves chegavam com hidropsia — acúmulo de líquido no abdome, no tórax, nos tecidos. Eram os mesmos bebês de Hipócrates.
O que eles tinham em comum? Ninguém sabia. E não saberia por muito tempo.
A chave estava no sangue — a descoberta do fator Rh
Em 1900, Karl Landsteiner — um médico austríaco que trabalhava em Viena — misturou amostras de sangue de pessoas diferentes e observou que algumas combinações causavam aglutinação: os glóbulos vermelhos se agrupavam e precipitavam. Outras combinações não causavam nada.
Ele havia descoberto os grupos sanguíneos. A, B, O — os primeiros três. Em 1902, Decastello e Sturli descreveram o quarto: AB. Landsteiner recebeu o Nobel de Medicina em 1930.
A descoberta foi revolucionária para a transfusão sanguínea, mas ainda não explicava as mortes dos bebês. Faltava uma peça.
Em 1940, Landsteiner — agora nos Estados Unidos — e Alexander Wiener descobriram outro sistema de grupos sanguíneos, ao injetar sangue de macaco Rhesus em coelhos e observar a reação. Chamaram o novo antígeno de fator Rh. A maioria das pessoas tem esse fator nas hemácias — são Rh positivas. Cerca de 15% não têm — são Rh negativas.
No ano seguinte, Philip Levine e colaboradores publicaram um achado que fecharia o círculo: a incompatibilidade Rh era responsável por 95% dos casos de doença hemolítica perinatal.
O mecanismo, finalmente, estava claro.
O que acontece na incompatibilidade Rh: mãe e bebê com tipos diferentes
Uma mãe Rh negativa que gesta um bebê Rh positivo (herdado do pai) enfrenta uma situação que o sistema imunológico trata como ameaça. No parto — ou em outros momentos em que sangue fetal entra na circulação materna, como sangramentos, amniocentese ou versão externa — o organismo da mãe entra em contato com as hemácias Rh positivas do bebê.
Reconhece-as como estranhas. Produz anticorpos anti-D.
Na primeira gestação, esse processo geralmente é silencioso — os anticorpos aparecem após o parto, quando o bebê já nasceu. Mas na gestação seguinte, esses anticorpos já estão em circulação. Eles atravessam a placenta, se ligam às hemácias do bebê Rh positivo e as destroem — processo chamado hemólise. O bebê desenvolve anemia progressiva. Se não tratado, pode desenvolver hidropsia e morrer. O mesmo mecanismo de anticorpos maternos atuando contra células fetais também explica parte das complicações em gestações gemelares, onde a síndrome de transfusão feto-fetal representa outro cenário de desequilíbrio entre circulações fetais — embora por mecanismo diferente.
São os bebês de Hipócrates, agora com nome e explicação.
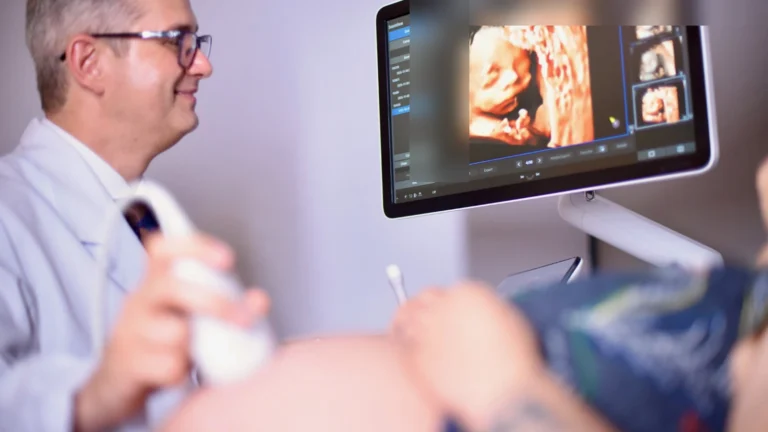
Aprender a enxergar sem entrar
Conhecer o mecanismo não era suficiente. Era preciso saber, durante a gestação, se o bebê estava sendo afetado — e com que gravidade.
Em 1945, Robin Coombs e colaboradores descreveram o teste de antiglobulina — o Teste de Coombs — capaz de detectar anticorpos ligados às hemácias. Esse exame ainda é usado hoje para identificar aloimunização materna.
Em 1953, Douglas Bevis demonstrou que o líquido amniótico de gestações afetadas continha bilirrubina — o produto da destruição das hemácias — em quantidades que variavam com a gravidade da anemia. A ideia de analisar o líquido amniótico começava a tomar forma.
Em 1961, o médico neozelandês William Liley descreveu um método para medir a quantidade de bilirrubina no líquido amniótico por espectrofotometria — a absorção de luz em comprimento de onda específico (450 nm) — e correlacionou esse valor com a gravidade da doença. Era a primeira ferramenta objetiva para monitorar anemia fetal antes do parto.
Dois anos depois, em 1963, Liley foi ainda mais longe: realizou a primeira transfusão intrauterina da história — guiada por raio-X, com acesso intraperitoneal — em um feto gravemente anêmico. O bebê sobreviveu. Era o início da medicina fetal como especialidade.
Em 1964, Vincent Freda e colegas realizaram a primeira transfusão intravascular em um feto de 26 semanas. Foi também, tecnicamente, o primeiro caso de cirurgia fetal aberta.
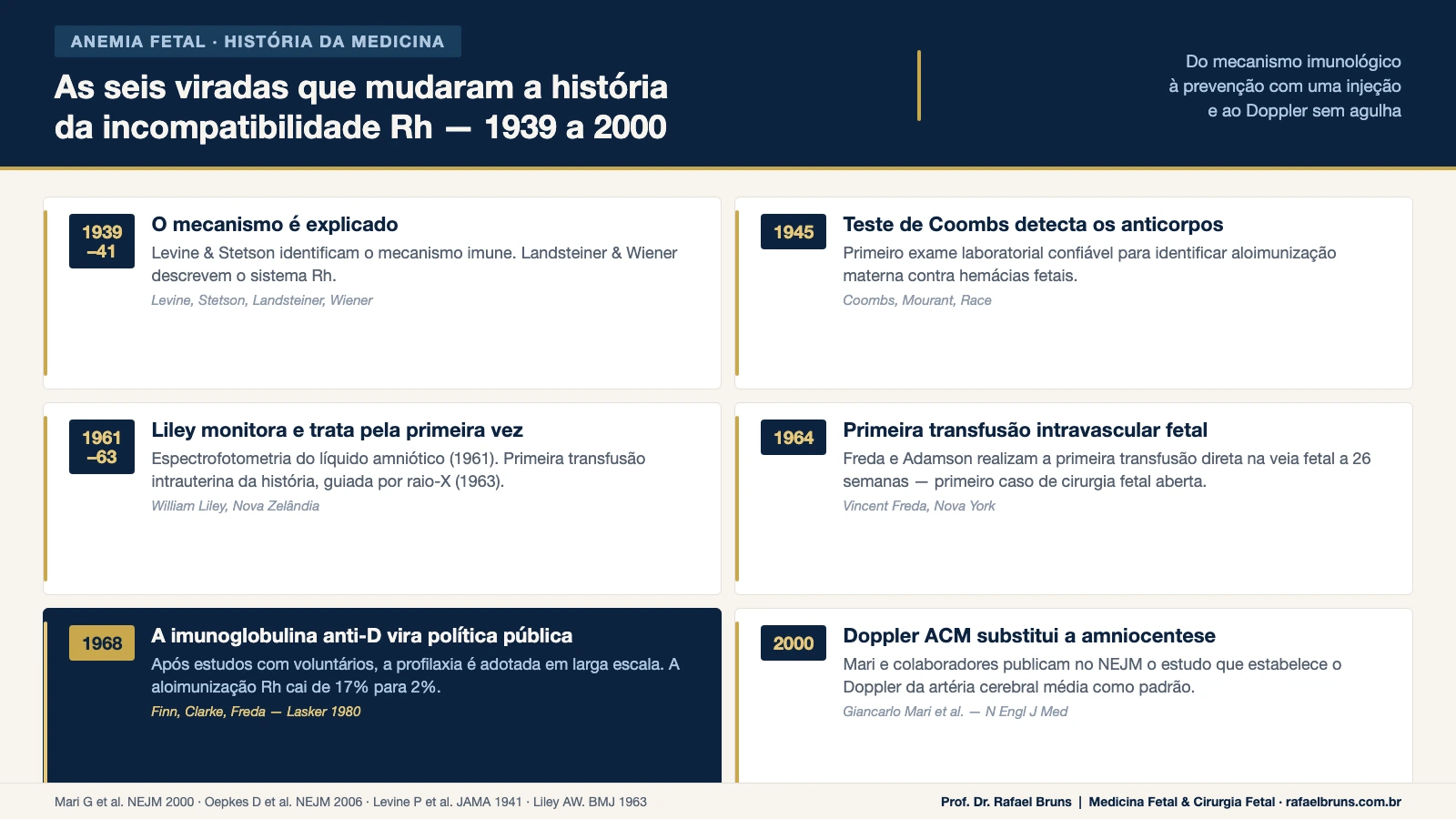
A maior virada: aprender a prevenir
Tratar era possível. Mas havia uma pergunta mais importante: dava para evitar que a mãe desenvolvesse anticorpos em primeiro lugar?
A resposta começou a tomar forma nos anos 1960, de forma simultânea em três continentes. Ronald Finn em Liverpool, Cyril Clarke no Reino Unido, e Vincent Freda em Nova York desenvolveram, independentemente, a hipótese de que injetar anticorpos anti-D passivos na mãe logo após o parto poderia suprimir a resposta imunológica — antes que ela tivesse tempo de se estabelecer.
A lógica era contraintuitiva mas elegante: dar à mãe os anticorpos prontos, para que eles “limpem” rapidamente as hemácias fetais que entraram em sua circulação no parto — sem dar tempo para o sistema imunológico ativá-las como ameaça e produzir memória imunológica.
Os experimentos em voluntários, entre 1960 e 1965, confirmaram a hipótese.
Em 1968, a profilaxia com imunoglobulina anti-D foi adotada como programa de saúde pública no Reino Unido e, logo depois, em diversos países. O efeito foi imediato e dramático: a taxa de aloimunização Rh caiu de 17% para 2% nas populações onde o programa foi implementado de forma consistente.
Uma das maiores causas de mortalidade neonatal da história tinha se tornado prevenível com uma injeção.
Freda, Gorman e Pollack receberam o Prêmio Lasker — considerado o Nobel americano da medicina — em 1980, pelo desenvolvimento da imunoglobulina anti-D.
James Harrison e o braço de ouro
A imunoglobulina anti-D precisa ser fabricada. E para fabricá-la, é necessária uma matéria-prima que não se sintetiza em laboratório: plasma humano com concentrações altas de anticorpos anti-D.
A maioria das pessoas produz esses anticorpos após contato com sangue Rh positivo — uma transfusão, um parto. São anticorpos comuns, mas em concentrações geralmente baixas. O que a indústria farmacêutica precisava era de doadores com níveis excepcionalmente altos e estáveis desses anticorpos no plasma.
Em 1954, um jovem australiano chamado James Harrison recebeu uma transfusão de sangue após uma cirurgia torácica complexa aos 14 anos de idade. Quando adulto, descobriu que o seu sangue tinha algo incomum: anticorpos anti-D em concentrações raramente vistas. Começou a doar plasma aos 18 anos.
Ele não parou por sessenta anos.
Harrison doou plasma mais de mil vezes ao longo de seis décadas. Seu plasma foi utilizado pela Cruz Vermelha Australiana para produzir imunoglobulina anti-D — a vacina, por assim dizer, que protege bebês de mães Rh negativas. As estimativas australianas indicam que suas doações contribuíram para salvar mais de dois milhões de bebês.
A imprensa australiana o chamou de “The Man with the Golden Arm” — o homem do braço de ouro.
“Harrison doou plasma mais de mil vezes ao longo de seis décadas. As estimativas australianas indicam que suas doações contribuíram para salvar mais de dois milhões de bebês.”
Em maio de 2018, aos 81 anos, Harrison fez sua última doação. Os médicos disseram que ele havia chegado ao limite de idade para doação. Ele saiu do centro de coleta como sempre — pelo mesmo braço.
O que a prevenção não resolve — e o que o Doppler completou
A imunoglobulina anti-D transformou a incompatibilidade Rh em uma condição amplamente prevenível — mas não completamente eliminada. Há situações em que a aloimunização ocorre apesar da profilaxia: doação insuficiente, falha de administração, exposição não identificada antes do parto, aloimunização por outros antígenos (Kell, Kidd, Duffy) que a imunoglobulina anti-D não cobre.
Nesses casos — e são dezenas de milhares de gestações por ano no mundo — o desafio volta a ser monitorar se o bebê está sendo afetado.
Por décadas, a ferramenta para isso foi a amniocentese com espectrofotometria — herdada de Liley. Útil, mas invasiva, com risco de ruptura de membranas, infecção e até piora da sensibilização.
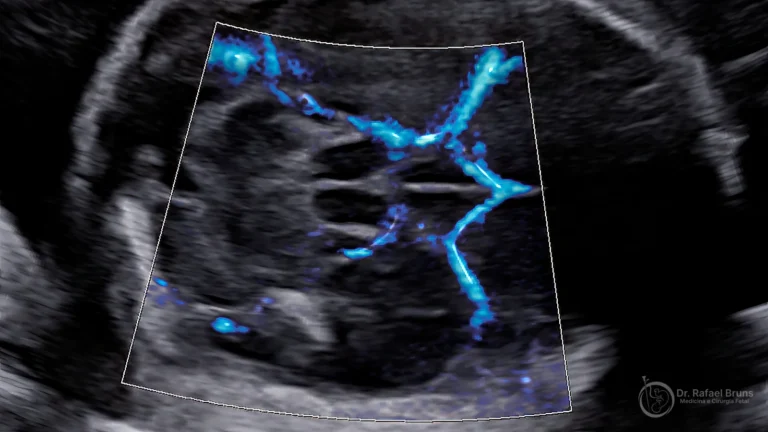
Em 2000, Giancarlo Mari e colaboradores publicaram no New England Journal of Medicine o estudo que estabeleceu um novo padrão: o Doppler da artéria cerebral média — um exame sem agulha, feito durante o ultrassom convencional — era capaz de detectar anemia fetal grave com confiabilidade suficiente para substituir a amniocentese. O valor de corte de 1,5 MoM foi definido nesse estudo.
Em 2006, o estudo DIAMOND, liderado pelo Prof. Dick Oepkes em Leiden, confirmou de forma definitiva a superioridade do Doppler: mais sensível, mais acurado, sem os riscos do procedimento invasivo.
Em 2015, tive a oportunidade de completar o Advanced Course in Fetoscopic Laser Surgery no Leiden University Medical Center, sob orientação do próprio Prof. Oepkes — um dos maiores especialistas mundiais em medicina fetal e coautor dos estudos que transformaram o manejo da síndrome de transfusão feto-fetal. A formação em Leiden conectou diretamente o que está descrito neste artigo — o Doppler, a transfusão intrauterina, o monitoramento não invasivo — com a prática clínica que realizamos hoje em Curitiba e Porto Alegre.

O arco estava completo: do mistério de Hipócrates à prevenção com uma injeção, e do monitoramento invasivo ao Doppler sem agulha. Em pouco mais de oitenta anos, uma doença que matava bebês por milênios havia sido compreendida, tratada e, na maior parte dos casos, prevenida.
O que isso significa hoje para gestantes Rh negativas
Se você é Rh negativa e está grávida, o protocolo atual é claro:
A imunoglobulina anti-D é administrada rotineiramente ao redor de 28 semanas e nas primeiras 72 horas após o parto, quando o bebê for Rh positivo. Em situações de sangramento, procedimentos invasivos ou trauma abdominal durante a gestação, uma dose adicional pode ser necessária.
Se a aloimunização já ocorreu — ou seja, se os anticorpos já estão presentes na circulação materna — o monitoramento por Doppler da artéria cerebral média entra no protocolo a partir do momento em que a titulação atinge o valor crítico. O exame é repetido a cada uma a duas semanas, dependendo do risco.
Quando o Doppler indica anemia significativa, a cordocentese confirma e a transfusão intrauterina trata. Liley abriria um sorriso.
O que mais impressiona nessa história não é nenhuma descoberta isolada. É a cadeia: cada resposta gerou a pergunta seguinte, cada tratamento revelou o que ainda faltava. De Hipócrates a James Harrison, do raio-X de Liley ao Doppler de Oepkes — a medicina construiu, tijolo por tijolo, algo que parece quase impossível: uma vitória contra uma doença que existia desde que existem seres humanos.
⚠ QUANDO BUSCAR AVALIAÇÃO ESPECIALIZADA
- Você descobriu que é Rh negativa e ainda não recebeu orientação sobre imunoglobulina anti-D
- Seus anticorpos anti-D (ou outros) foram detectados e a titulação está subindo
- O Doppler da artéria cerebral média mostrou velocidade acima de 1,5 MoM
- Você está em uma segunda gestação ou mais, e teve sensibilização em gestação anterior
- O bebê apresenta sinais de hidropsia ou anemia no ultrassom
Atendimento presencial em Curitiba e Porto Alegre. Teleconsulta disponível para pacientes de qualquer estado — Resolução CFM 2.314/2022.
Perguntas frequentes
Referências
- Landsteiner K, Wiener AS. An agglutinable factor in human blood recognized by immune sera for Rhesus blood. Proc Soc Exp Biol Med. 1940;43:223.
- Levine P, Katzin EM, Burnham L. Isoimmunization in pregnancy: its possible bearing on the etiology of erythroblastosis fetalis. JAMA. 1941;116:825–827.
- Coombs RRA, Mourant AE, Race RR. A new test for the detection of weak and incomplete Rh agglutinins. Br J Exp Pathol. 1945;26:255–266.
- Liley AW. Liquor amnii analysis in the management of the pregnancy complicated by Rhesus sensitization. Am J Obstet Gynecol. 1961;82:1359–1370.
- Liley AW. Intrauterine transfusion of foetus in haemolytic disease. Br Med J. 1963;5365:1107–1109.
- Freda VJ, Adamson SK Jr. Exchange transfusion in utero: report of a case. Am J Obstet Gynecol. 1964;89:817–821.
- Freda VJ, Gorman JG, Pollack W. Successful prevention of experimental Rh sensitization in man with an Anti-Rh Gamma2-Globulin antibody preparation. Transfusion. 1964;4:26–32.
- Mari G, Deter RL, Carpenter RL, et al. Noninvasive diagnosis by Doppler ultrasonography of fetal anemia due to maternal red-cell alloimmunization. Collaborative Group for Doppler Assessment of the Blood Velocity in Anemic Fetuses. N Engl J Med. 2000;342(1):9–14.
- Oepkes D, Seaward PG, Vandenbussche FP, et al. Doppler ultrasonography versus amniocentesis to predict fetal anemia. DIAMOND Study Group. N Engl J Med. 2006;355(2):156–164.
Conteúdo informativo. Não substitui consulta médica presencial ou por telemedicina com avaliação individualizada. Prof. Dr. Rafael Frederico Bruns — CRM-PR | CRM-RS. Medicina Fetal e Cirurgia Fetal.